uzsver
Krustnagliņa ir plaši atzīta par ieguvumiem veselībai, un to bieži lieto vēža pacienti un tie, kuriem ir ģenētisks risks. Tomēr Clove drošība un efektivitāte vēža slimniekiem ir atkarīga no daudziem faktoriem, piemēram, vēža indikācijām, ķīmijterapijas, citām ārstēšanas metodēm un audzēja ģenētikas. Ir ļoti svarīgi zināt, ka daži pārtikas produkti un uztura bagātinātāji, piemēram, greipfrūti un spināti, var slikti mijiedarboties ar vēža zālēm un izraisīt nevēlamas reakcijas.
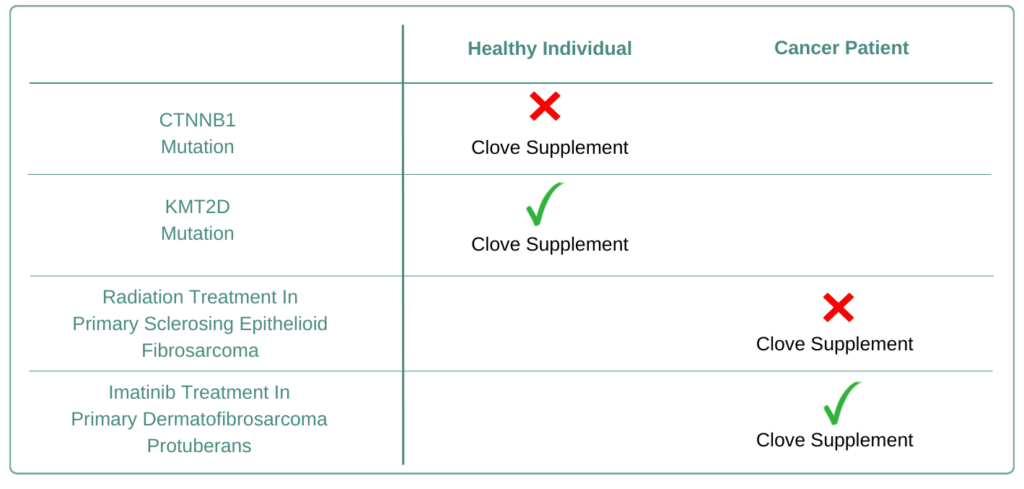
Diētai ir izšķiroša nozīme vēža ārstēšanā, jo tā var ietekmēt ārstēšanas rezultātus. Vēža slimniekiem rūpīgi jāizvēlas un savā uzturā jāiekļauj piemēroti pārtikas produkti un uztura bagātinātāji. Piemēram, krustnagliņa varētu būt noderīga tiem, kuriem ir primārā dermatofibrosarkoma Protuberans un kuriem tiek veikts imatinibs, taču tas var nebūt piemērots pacientiem, kuri saņem starojumu primārās sklerozējošās epitēlija fibrosarkomas ārstēšanai. Turklāt, lai gan krustnagliņa varētu palīdzēt personām ar ģenētisko riska faktoru “KMT2D”, to nedrīkst ieteikt tiem, kam ir atšķirīgs ģenētiskais risks “CTNNB1”. Ir svarīgi personalizēt uztura plānus, pamatojoties uz veselību, ārstēšanu un ģenētiku.
Izšķiroša nozīme ir izpratnei par to, ka, pieņemot lēmumu par krustnagliņu piemērotību vēža slimniekam, ir jābūt individualizētam. Kritiskie faktori, piemēram, vēža veids, ārstēšanas metodes, ģenētiskā uzbūve, ģenētiskie riski, vecums, ķermeņa svars un dzīvesveids, ir ļoti svarīgi, lai izlemtu, vai krustnagliņa ir pareizā izvēle. Īpaši svarīgs apsvērums ir ģenētika un genomika. Tā kā šie faktori var mainīties, ir svarīgi regulāri pārskatīt un pielāgot uztura izvēli, lai tā atbilstu izmaiņām veselības stāvoklī un ārstēšanā.
Noslēgumā jāsaka, ka holistiska pieeja uztura izvēlei ir ļoti svarīga, koncentrējoties uz visu aktīvo sastāvdaļu kopējo ietekmi pārtikas produktos/piedevās, piemēram, krustnagliņās, nevis novērtējot katru aktīvo sastāvdaļu atsevišķi vai pilnībā to ignorējot. Šī plašā perspektīva veicina racionālāku un zinātniskāku pieeju vēža uztura plānošanai.
Īss pārskats
Vēža slimnieku vidū pieaug augu izcelsmes pārtikas un uztura bagātinātāju, piemēram, vitamīnu, augu, minerālvielu, probiotiku un dažādu specializētu uztura bagātinātāju, lietošana. Šie uztura bagātinātāji ir paredzēti, lai nodrošinātu augstu specifisku aktīvo sastāvdaļu koncentrāciju, no kurām daudzas ir arī dažādos pārtikas produktos. Aktīvo sastāvdaļu koncentrācija un daudzveidība veseliem pārtikas produktiem un uztura bagātinātājiem atšķiras. Pārtikas produkti parasti piedāvā virkni aktīvo sastāvdaļu, bet zemākās koncentrācijās, savukārt uztura bagātinātāji nodrošina lielāku konkrētu sastāvdaļu koncentrāciju.
Ņemot vērā katras aktīvās sastāvdaļas dažādās zinātniskās un bioloģiskās funkcijas molekulārā līmenī, ir ļoti svarīgi ņemt vērā šo komponentu kopējo ietekmi, lemjot par pārtikas produktiem un uztura bagātinātājiem, ko ēst vai ne.

Rodas kritisks jautājums: vai krustnagliņas jāiekļauj savā uzturā kā pārtikas produkts vai papildinājums? Vai ir ieteicams lietot krustnagliņu, ja jums ir ģenētiska nosliece uz vēzi, kas saistīta ar KMT2D gēnu? Ko darīt, ja jūsu ģenētiskais risks izriet no CTNNB1 gēna? Vai ir lietderīgi iekļaut savā uzturā krustnagliņu, ja jums ir diagnosticēta primārā sklerozējošā epitēlija fibrosarkoma vai primārā dermatofibrosarkoma protuberans? Turklāt, kā būtu jāpielāgo jūsu krustnagliņu patēriņš, ja jūs saņemat ārstēšanu ar imatinibu vai ja jūsu ārstēšanas plāns pāriet no imatiniba uz radiāciju? Ir svarīgi atzīt, ka ar tādiem vienkāršotiem apgalvojumiem kā “krustnagliņa ir dabiska, tāpēc tā vienmēr ir noderīga” vai “krustnagliņa uzlabo imunitāti” nepietiek, lai apzināti izvēlētos pārtiku/piedevas.
Turklāt ir svarīgi atkārtoti novērtēt krustnagliņu iekļaušanas uzturā piemērotību, ja tiek veiktas izmaiņas ārstēšanas shēmā. Rezumējot, pieņemot lēmumus par pārtikas produktu vai piedevu, piemēram, krustnagliņu, iekļaušanu uzturā, lai gūtu labumu no tā, ir jāņem vērā visu sastāvdaļu kopējā bioķīmiskā iedarbība, ņemot vērā tādus faktorus kā vēža veids, specifiskā ārstēšana, ģenētiskā nosliece. un dzīvesveida izvēli.
vēzis
Vēzis joprojām ir nozīmīgs izaicinājums medicīnas jomā, bieži izraisot plašu trauksmi. Tomēr jaunākie sasniegumi ir uzlabojuši ārstēšanas rezultātus, jo īpaši izmantojot personalizētas ārstēšanas pieejas, neinvazīvas uzraudzības metodes, izmantojot asins un siekalu paraugus, un imūnterapijas attīstību. Agrīna atklāšana un savlaicīga iejaukšanās ir bijusi ļoti svarīga, lai pozitīvi ietekmētu vispārējos ārstēšanas rezultātus.
Ģenētiskā pārbaude piedāvā nozīmīgu solījumu agrīnā vēža riska un jutības novērtēšanā. Tomēr daudziem cilvēkiem ar ģimenes un ģenētisku noslieci uz vēzi, terapeitiskās iejaukšanās iespējas, pat ar regulāru uzraudzību, bieži vien ir ierobežotas vai vispār nav. Kad ir diagnosticēts noteikts vēža veids, piemēram, primārā dermatofibrosarkoma protuberans vai primārā sklerozējošā epitēlija fibrosarkoma, ārstēšanas stratēģijas ir jāpielāgo, pamatojoties uz indivīda audzēja ģenētiku, slimības stadiju, kā arī tādiem faktoriem kā vecums un dzimums.
Pastāvīga uzraudzība pēc ārstēšanas ir būtiska, lai atklātu jebkādas vēža recidīva pazīmes un informētu par turpmākiem lēmumiem. Daudzi vēža pacienti un riska grupas pacienti bieži meklē padomu par noteiktu pārtikas produktu un uztura bagātinātāju iekļaušanu savā uzturā, kam ir izšķiroša nozīme viņu vispārējā lēmumu pieņemšanas procesā par veselības pārvaldību.
Kritiskais jautājums ir, vai, lemjot par uztura izvēli, piemēram, krustnagliņu, ņemt vērā ģenētiskos riskus un specifiskas vēža diagnozes. Vai ģenētiskajam vēža riskam, kas izriet no mutācijas KMT2D, ir tāda pati ietekme uz bioķīmisko ceļu kā mutācijai CTNNB1? No uztura viedokļa vai risks, kas saistīts ar primāro dermatofibrosarkomu Protuberans, ir līdzvērtīgs primārai sklerozējošai epitēlija fibrosarkomai? Turklāt, vai tiem, kam tiek veikta radiācija, uztura ievērošana paliek tāda pati kā tiem, kas saņem imatinibu? Šie apsvērumi ir ļoti svarīgi, lai izdarītu apzinātu pārtikas izvēli personām ar dažādu ģenētisko risku un vēža ārstēšanu.
Krustnagliņa – uztura bagātinātājs
Papildinājums krustnagliņa ietver virkni aktīvo sastāvdaļu, tostarp K vitamīnu, A vitamīnu, palmitīnskābi, oleīnskābi un oleanolskābi, katrai no tām ir dažādas koncentrācijas. Šīs sastāvdaļas ietekmē molekulāros ceļus, īpaši PI3K-AKT-MTOR signalizāciju, TGFB signalizāciju, fokusa adhēziju un DAP12 signalizāciju, kas regulē vēža kritiskos aspektus šūnu līmenī, piemēram, audzēja augšanu, izplatīšanos un šūnu nāvi. Ņemot vērā šo bioloģisko ietekmi, atbilstošu uztura bagātinātāju, piemēram, krustnagliņas, izvēle atsevišķi vai kombinācijā kļūst par kritisku lēmumu vēža uztura kontekstā. Apsverot iespēju lietot krustnagliņu vēža ārstēšanai, ir svarīgi ņemt vērā šos dažādos faktorus un mehānismus. Tas ir tāpēc, ka līdzīgi kā vēža ārstēšanā krustnagliņu lietošana nav universāls lēmums, kas piemērots visiem vēža veidiem, bet tas ir jāpielāgo.
Krustnagliņu piedevu izvēle
Atbildēt uz jautājumu “Kad man vajadzētu izvairīties no krustnagliņas vēža kontekstā” ir sarežģīti, jo atbilde ir ļoti individualizēta – tā vienkārši ir “Atkarīgs!”. Līdzīgi kā jebkura vēža ārstēšana var nebūt efektīva katram pacientam, Clove atbilstība un drošība vai ieguvumi atšķiras atkarībā no personīgajiem apstākļiem. Tādi faktori kā konkrētais vēža veids, ģenētiskās noslieces, pašreizējās ārstēšanas metodes, citi uztura bagātinātāji, dzīvesveida paradumi, ĶMI un jebkādas alerģijas ietekmē, lai noteiktu, vai krustnagliņa ir piemērota vai no tā jāizvairās, uzsverot, cik svarīgi ir individuāli apsvērt šādus lēmumus.
Ēdieni, kas jāēd pēc vēža diagnostikas!
Nav divu vienādu vēža veidu. Pārsniedziet kopīgās uztura vadlīnijas ikvienam un ar pārliecību pieņemiet personalizētus lēmumus par pārtiku un uztura bagātinātājiem.
1. Vai krustnagliņu piedevas dos labumu primārās sklerozējošās epitēlija fibrosarkomas pacientiem, kuriem tiek veikta staru terapija?
Primāro sklerozējošo epitēlija fibrosarkomu raksturo īpašas ģenētiskas mutācijas, proti, PBRM1, ATRX un PIK3C2G, kas izraisa izmaiņas bioķīmiskajos ceļos, īpaši TGFB signalizācijā un inozīta fosfāta signalizācijā. Vēža ārstēšanas, piemēram, staru terapijas, efektivitāte ir atkarīga no tā darbības mehānisma šajos konkrētajos ceļos. Ideālā stratēģija ietver ārstēšanas darbības saskaņošanu ar ceļiem, kas izraisa vēzi, tādējādi nodrošinot personalizētu un efektīvu pieeju. Šādos scenārijos ir ļoti svarīgi izvairīties no pārtikas produktiem vai uztura bagātinātājiem, kas varētu neitralizēt ārstēšanas ietekmi vai mazināt šo pielīdzināšanu. Piemēram, krustnagliņu piedeva, kas ietekmē TGFB signālu, var nebūt pareizā izvēle primārās sklerozējošās epitēlija fibrosarkomas gadījumā, kad tiek pakļauta radiācijai. Tas ir tāpēc, ka tas var vai nu saasināt slimības progresēšanu, vai traucēt ārstēšanas efektivitāti. Izvēloties uztura plānu, ir svarīgi ņemt vērā tādus faktorus kā vēža veids, notiekošā ārstēšana, vecums, dzimums, ĶMI, dzīvesveids un visas zināmās ģenētiskās mutācijas.
2. Vai krustnagliņu piedevas dos labumu primārās dermatofibrosarkomas protuberānas pacientiem, kuriem tiek veikta imatiniba terapija?
Primārā dermatofibrosarkoma Protuberans tiek identificēta ar specifiskām ģenētiskām mutācijām, piemēram, FGFR1, KDM5A un MED12, kuru rezultātā mainās bioķīmiskie ceļi, īpaši PI3K-AKT-MTOR signalizācija, angioģenēze, MAPK signalizācija, onkogēnā histona metilēšana un TGFB signalizācija. Vēža ārstēšanas, piemēram, imatiniba, efektivitāti nosaka tā mijiedarbība ar šiem ceļiem. Mērķis ir nodrošināt, lai ārstēšana būtu labi saskaņota ar ceļiem, kas izraisa vēzi, nodrošinot personalizētu ārstēšanas pieeju. Šajā kontekstā jāapsver pārtikas produkti vai uztura bagātinātāji, kas ir saderīgi ar ārstēšanu vai uzlabo šo pielīdzināšanu. Piemēram, krustnagliņu piedeva ir racionāla izvēle tiem, kam ir primārā dermatofibrosarkoma protuberans un tiek ārstēts imatinibs. Tas ir tāpēc, ka krustnagliņa ietekmē tādus ceļus kā PI3K-AKT-MTOR signalizācija, kas var vai nu kavēt faktorus, kas izraisa primāro dermatofibrosarcoma protuberans, vai arī uzlabot imatiniba efektivitāti.
3. Vai krustnagliņu piedevas ir drošas veselām personām ar CTNNB1 mutāciju saistītu ģenētisko risku?
Dažādi uzņēmumi nodrošina gēnu paneļus dažādu vēža veidu ģenētiskā riska novērtēšanai. Šajos paneļos ir gēni, kas saistīti ar krūts, olnīcu, dzemdes, prostatas un kuņģa-zarnu trakta vēzi. Šo gēnu pārbaude var apstiprināt diagnozi un informēt par ārstēšanas un pārvaldības stratēģijām. Varianta identificēšana, kas izraisa slimību, var vēl vairāk palīdzēt pārbaudīt un diagnosticēt radiniekus, kuri var būt apdraudēti. CTNNB1 gēns parasti ir iekļauts šajos paneļos vēža riska novērtēšanai.
CTNNB1 gēna mutācija ietekmē bioķīmiskos ceļus vai procesus, piemēram, fokusa adhēziju, Adherena savienojumu un epitēlija–mezenhimālo pāreju, kas ir tieši vai netieši iesaistīti vēža izraisīšanā molekulārā līmenī. Kad ģenētiskais panelis identificē CTNNB1 mutāciju, kas saistīta ar paaugstinātu virsnieru garozas karcinomas risku, zinātniskais pamatojums liecina, ka jāizvairās no piedevas Clove lietošanas. Tas ir tāpēc, ka krustnagliņu piedeva ietekmē tādus ceļus kā fokusa adhēzija, kas var izraisīt negatīvas sekas CTNNB1 mutācijas un ar to saistīto vēža stāvokļu kontekstā.
4. Vai krustnagliņu piedevas ir drošas veselām personām ar KMT2D mutāciju saistītu ģenētisko risku?
KMT2D ir izšķiroša loma vēža riska novērtēšanā. KMT2D mutācijas var izjaukt kritiskos bioķīmiskos ceļus, tostarp DAP12 signalizāciju un onkogēno histonu metilēšanu, kas ietekmē vēža attīstību. Ja jūsu ģenētiskais panelis atklāj KMT2D mutācijas, kas saistītas ar urīnpūšļa urotēlija karcinomu, apsveriet iespēju iekļaut savā uztura plānā krustnagliņu piedevas. Šie papildinājumi var pozitīvi ietekmēt ceļus, piemēram, DAP12 signalizāciju, sniedzot atbilstošu atbalstu personām ar KMT2D mutācijām un ar to saistītām veselības problēmām.
Secinājums
Divas vissvarīgākās lietas, kas jāatceras, ir tādas, ka vēža ārstēšana un uzturs nekad nav vienādi visiem. Uzturs, tostarp pārtika un uztura bagātinātāji, piemēram, krustnagliņa, ir efektīvs līdzeklis, ko jūs varat kontrolēt, saskaroties ar vēzi.
"Ko man vajadzētu ēst?" ir visbiežāk uzdotais jautājums, ko uzdod vēža pacienti un tie, kuriem ir vēža risks. Pareizā atbilde ir tāda, ka tā ir atkarīga no tādiem faktoriem kā vēža veids, audzēja ģenētika, pašreizējā ārstēšana, alerģijas, dzīvesveids un ĶMI.
Iegūstiet savu uztura personalizēšanu vēža ārstēšanai no addon, noklikšķinot uz tālāk esošās saites un atbildot uz jautājumiem par vēža veidu, ārstēšanu, dzīvesveidu, alerģijām, vecumu un dzimumu.
Personalizēts uzturs vēža ārstēšanai!
Vēzis laika gaitā mainās. Pielāgojiet un mainiet savu uzturu, pamatojoties uz vēža indikācijām, ārstēšanu, dzīvesveidu, pārtikas izvēlēm, alerģijām un citiem faktoriem.
Atsauces
- cBioPortāls vēža genomikai
- Kompensējošā PI3-kināzes/Akt/mTor aktivācija regulē imatiniba rezistences attīstību.
- Retīnskābe, GABA-ergic un TGF-beta signalizācijas sistēmas ir iesaistītas cilvēka aukslēju šķeltnes fibroblastu fenotipā.
- Radio rezistence krūts vēža šūnās ir saistīta ar TGF-β signalizāciju, hibrīda epitēlija-mezenhimālo fenotipu un vēža cilmes šūnām.
- Oleīnskābes izraisītais ANGPTL4 uzlabo galvas un kakla plakanšūnu karcinomas anoikis rezistenci un metastāzes, pastiprinot fibronektīna regulēšanu.
- Metastātiskā vēža mutācijas ainava atklājās no iespējamās 10,000 XNUMX pacientu klīniskās secības.
- Oleīnskābe izraisa apoptozi un autofagiju, ārstējot mēles plakanšūnu karcinomas.
